
Kiến thức về hóa học là kiến thức quan trọng đối với mọi người. Đặc biệt đối với phương trình phản ứng, đây là thông tin cần nắm rõ. Vì vậy, hôm nay chúng tôi sẽ mang đến bài viết về phản ứng ion thu gọn để mọi người củng cố lại những kiến thức quan trọng. Hãy cùng chúng tôi bổ sung kiến thức qua bài viết dưới đây.

Khái niệm về phương trình ion thu gọn
Phương trình ion rút gọn của phản ứng sẽ cho biết nó xảy ra như thế nào trong dung dịch điện phân.
Lưu ý khi viết phương trình ion thu gọn
Để viết phương trình ion thu gọn, bạn phải có kiến thức vững chắc về độ tan, chất cố định, chất điện li yếu và thứ tự xuất hiện các chất trong dung dịch.
Khi viết phương trình ion, chất rắn, chất khí, chất lỏng được viết dưới dạng phân tử. Chất tan trong dung dịch gọi là ion
Phương trình ion thu gọn là phương trình hóa học trong đó các ion kết hợp với nhau.
Các bước viết phương trình ion thu gọn như sau:
– Bước 1: Viết phương trình phân tử của các chất phản ứng và sản phẩm (nhớ cân bằng phương trình).
– Bước 2: Chất điện li mạnh được liệt vào dạng ion. Chất không tan, chất khí và chất điện li yếu được viết dưới dạng phân tử => phương trình ion hoàn chỉnh.
– Bước 3: Khử các ion giống nhau ở 2 vế => phương trình ion thu gọn.
* Nếu một bài toán có nhiều hỗn hợp các nguyên tố nhưng có cùng phương trình khử thì có thể dùng phương trình ion rút gọn để tính bazơ của bài toán và giải bài toán một cách trọn vẹn, nhanh chóng.
* Khi xuất hiện hỗn hợp axit, bazơ với nhau thì phải dùng phương trình ion H+ + OH – → H2O để giải.
Các dạng bài tập và cách giải phương trình ion thu gọn
Chúng ta có thể sử dụng phương trình ion rút gọn để giải các bài toán về phản ứng axit-bazơ, phản ứng hòa tan hiđroxit lưỡng tính, oxit axit tác dụng với bazơ, phản ứng với không khí, phản ứng oxi hóa.
Các giải pháp
– Tính số đồ dùng đã cung cấp trong bài
– Cần xác định số hạt của các ion cần
Viết phương trình ion rút gọn của phản ứng
– Tính theo phương trình ion
– Từ đó sẽ tính được các đại lượng cần thiết như: lượng không khí, lượng muối, pH của dung dịch, loại chất khử,…
II. Các dạng phản ứng khi sử dụng phương trình ion rút gọn
Phản ứng giữa axit và bazơ: (Phản ứng trung hòa)
Phương trình phân tử của nó là:
HCl + NaOH → NaCl + H2O
H2SO4 + 2KOH → K2SO4 + 2H2O
– Phương trình ion:
H + + Cl – + Na + → Cl – + Na + + + H2O
2H+ + SO42– + 2K+ + 2OH – → SO42– + 2K+ + + H2O
Phương trình ion thu gọn là:
H + + OH – → H2O
Theo phương trình ion rút gọn: nH+ = noOH –
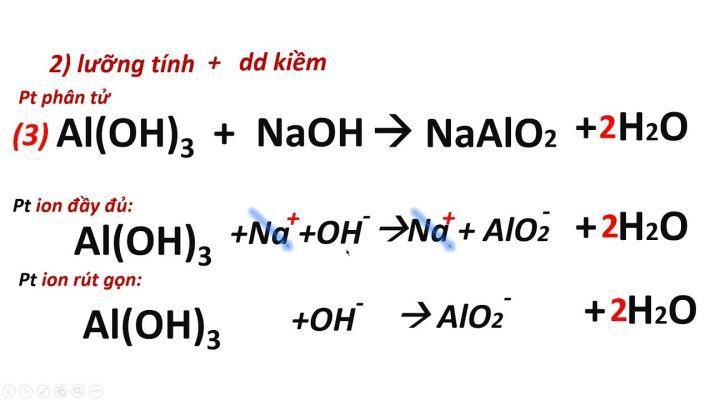
Phản ứng oxit axit và kiềm
– Xét nghiệm phân tử:
CO2 + 2KOH → K2CO3 + H2O
Hoặc CO2 + KOH → KHCO3
– Phương trình ion: CO2 + 2K + + + 2OH – → 2K + + CO32 – + H2O
Hoặc CO2 + K+ + OH– → K+ + HCO3–
Phương trình ion thu gọn:
CO2 + 2OH – → CO32 – + H2O
Hoặc CO2 + OH – → HCO3 –
Phản ứng giữa axit và muối
- Nếu ta cho từ từ axit vào muối cacbonat
– Xét nghiệm phân tử:
HCl + Na2CO3 → NaHCO3 + NaCl
HCl + NaHCO3 → NaCl + CO2 + H2O
– Phương trình ion:
H+ + Cl– + 2N a+ + CO32–→ Na+ + HCO3– + Na+ + Cl–
H+ + Cl – + HCO3 – + Na+ → Na+ + Cl – + CO2 + H2O
Phương trình ion thu gọn là:
H+ + CO32 – → HCO3 –
HCO3 – + H + → CO2 + H2O
- Nếu cho từ từ muối cacbonat vào axit
– Công thức phân tử: 2HCl + Na2CO3 → 2NaCl + CO2 + H2O
– Phương trình ion: 2H+ + 2C l– + 2N a+ + CO32–→ 2N a+ + 2C l– + CO2 + H2O
– Phương trình ion rút gọn: 2H+ + CO32 – → H2O + CO2

- Nếu chúng ta thêm một muối khác vào axit:
– Phương trình phân tử: HCl + AgNO3 → AgCl + HNO3
– Phương trình ion: H+ + Cl– + Ag+ + NO3–→ AgCl + H+ + NO3–
– Phương trình ion thu gọn: Cl – + Ag + → AgCl
Tác dụng của hai phương pháp muối với nhau
– Xét nghiệm phân tử:
Na2CO3 + MgCl2 → MgCO3 + 2NaCl
– Phương trình ion:
2Na+ + CO32–+ Mg2+ + Cl–→ MgCO3 + 2Na+ + + 2Cl–
Phương trình ion thu gọn:
CO32 – + Mg2+ → MgCO3
– Xét nghiệm phân tử:
Fe2(SO4)3 + 3Pb(NO3)2 → 2Fe(NO3)3 + 3PbSO4
– Phương trình ion
2Fe3+ + 3SO42 – + 3Pb2+ + 6NO3 – → 2Fe3+ + 6NO3 – + 3PbSO4
Phương trình ion thu gọn:
Pb2+ + SO42 – → PbSO4
kim loại có tính axit
– Xét nghiệm phân tử:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
– Phương trình ion:
2Cu + 8H+ + 8NO3 – → 3Cu2+ + 6NO3 – + 2NO + 4H2O
Phương trình ion thu gọn:
3Cu + 8H+ + 2NO3 – → 3Cu2+ + 2NO + 4H2O
oxit bazơ axit
– Xét nghiệm phân tử:
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
– Phương trình ion:
Fe2O3 + 6H+ + 3SO42 – → 2Fe3+ + 3SO42 – + 3H2O
Phương trình ion thu gọn:
Fe2O3 + 6H+ → 2Fe3+ + 3H2O
Kết thúc
Kiến thức cơ bản về phương trình ion rút gọn cho phản ứng trên. Hi vọng những thông tin này sẽ giúp mọi người thu thập được những thông tin quan trọng trong việc xin làm bài tập hay ứng dụng trong cuộc sống. Hãy chia sẻ thông tin này với mọi người xung quanh.
Bạn thấy bài viết phương trình ion rút gọn của phản ứng cho biết có khắc phục đươc vấn đề bạn tìm hiểu ko?, nếu ko hãy comment góp ý thêm về phương trình ion rút gọn của phản ứng cho biết bên dưới để Trường Đại học Đại Việt Sài Gòn có thể thay đổi & cải thiện nội dung tốt hơn cho các bạn nhé! Cám ơn bạn đã ghé thăm Website: daihocdaivietsaigon.edu.vn của Trường Đại học Đại Việt Sài Gòn
Nhớ để nguồn bài viết này: phương trình ion rút gọn của phản ứng cho biết của website daihocdaivietsaigon.edu.vn
Chuyên mục: Giáo Dục
Tóp 10 phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
Video phương trình ion rút gọn của phản ứng cho biết
Hình Ảnh phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
Tin tức phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
Review phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
Tham khảo phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
Mới nhất phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
Hướng dẫn phương trình ion rút gọn của phản ứng cho biết
#phương #trình #ion #rút #gọn #của #phản #ứng #cho #biết
